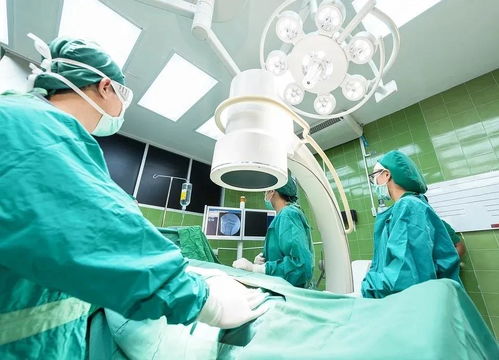
新《藥品管理法》配套規(guī)章制修訂啟動(dòng) 醫(yī)療器械研發(fā)迎來(lái)新機(jī)遇與挑戰(zhàn)

隨著新修訂的《藥品管理法》正式實(shí)施,其配套規(guī)章的制修訂工作已全面啟動(dòng)。這一舉措不僅為藥品行業(yè)帶來(lái)深刻變革,也為醫(yī)療器械的研發(fā)領(lǐng)域注入了新的活力與規(guī)范要求。新法規(guī)體系強(qiáng)調(diào)全生命周期管理、風(fēng)險(xiǎn)控制和創(chuàng)新激勵(lì),正推動(dòng)醫(yī)療器械研發(fā)從“跟跑”向“并跑”乃至“領(lǐng)跑”轉(zhuǎn)變。
一方面,新規(guī)加強(qiáng)了對(duì)醫(yī)療器械研發(fā)的監(jiān)管要求。研發(fā)過(guò)程中需更注重臨床數(shù)據(jù)真實(shí)性、安全性和有效性評(píng)價(jià),強(qiáng)化對(duì)高風(fēng)險(xiǎn)醫(yī)療器械的審評(píng)審批。例如,對(duì)人工智能輔助診斷設(shè)備、植入式器械等創(chuàng)新產(chǎn)品,明確了更嚴(yán)格的技術(shù)審查與倫理審查標(biāo)準(zhǔn),確保患者權(quán)益不受侵害。法規(guī)鼓勵(lì)采用真實(shí)世界數(shù)據(jù)等新型證據(jù)支持產(chǎn)品上市,為研發(fā)路徑提供了更多靈活性。
另一方面,配套規(guī)章也釋放出對(duì)創(chuàng)新的積極信號(hào)。通過(guò)優(yōu)化臨床試驗(yàn)審批流程、設(shè)立醫(yī)療器械創(chuàng)新綠色通道、加強(qiáng)知識(shí)產(chǎn)權(quán)保護(hù)等措施,大幅降低了研發(fā)制度性成本。特別是對(duì)中小型科技企業(yè),新規(guī)通過(guò)簡(jiǎn)化注冊(cè)程序、提供技術(shù)指導(dǎo)服務(wù),助力其將創(chuàng)新成果快速轉(zhuǎn)化為市場(chǎng)產(chǎn)品。法規(guī)還推動(dòng)產(chǎn)學(xué)研醫(yī)深度融合,支持聯(lián)合研發(fā)平臺(tái)建設(shè),促進(jìn)高端醫(yī)療器械國(guó)產(chǎn)化突破。
值得注意的是,醫(yī)療器械研發(fā)正面臨全球化競(jìng)爭(zhēng)與技術(shù)迭代加速的雙重挑戰(zhàn)。新規(guī)要求企業(yè)不僅要關(guān)注國(guó)內(nèi)標(biāo)準(zhǔn),還需對(duì)接國(guó)際醫(yī)療器械法規(guī)(如歐盟MDR、美國(guó)FDA要求),推動(dòng)研發(fā)體系與國(guó)際接軌。在人工智能、納米材料、生物3D打印等前沿領(lǐng)域,法規(guī)與科技發(fā)展的同步性將成為影響研發(fā)效能的關(guān)鍵因素。
隨著配套規(guī)章的逐步完善,醫(yī)療器械研發(fā)將呈現(xiàn)三大趨勢(shì):一是“智能化”研發(fā)成為主流,大數(shù)據(jù)與AI技術(shù)將深度融合于產(chǎn)品設(shè)計(jì)優(yōu)化階段;二是“精準(zhǔn)化”需求凸顯,個(gè)性化定制器械研發(fā)將迎來(lái)政策支持;三是“全鏈條”責(zé)任強(qiáng)化,企業(yè)需建立覆蓋研發(fā)、生產(chǎn)、流通、使用的全程質(zhì)量管理體系。
新《藥品管理法》配套規(guī)章的制修訂,為醫(yī)療器械研發(fā)構(gòu)筑了更科學(xué)、嚴(yán)謹(jǐn)且充滿(mǎn)活力的制度環(huán)境。企業(yè)與科研機(jī)構(gòu)應(yīng)主動(dòng)適應(yīng)法規(guī)變化,將合規(guī)要求內(nèi)化為研發(fā)核心競(jìng)爭(zhēng)力,共同推動(dòng)我國(guó)醫(yī)療器械行業(yè)向高質(zhì)量發(fā)展邁進(jìn)。
如若轉(zhuǎn)載,請(qǐng)注明出處:http://m.joryherb.cn/product/16.html
更新時(shí)間:2026-05-06 10:24:00